compuesto de coordinación, cualquiera de una clase de sustancias con estructuras químicas en las que un átomo metálico central está rodeado por átomos o grupos de átomos no metálicos, llamados ligandos, unidos a él mediante enlaces químicos. Los compuestos de coordinación incluyen sustancias como la vitamina B12, la hemoglobina y la clorofila, colorantes y pigmentos y catalizadores utilizados en la preparación de sustancias orgánicas.
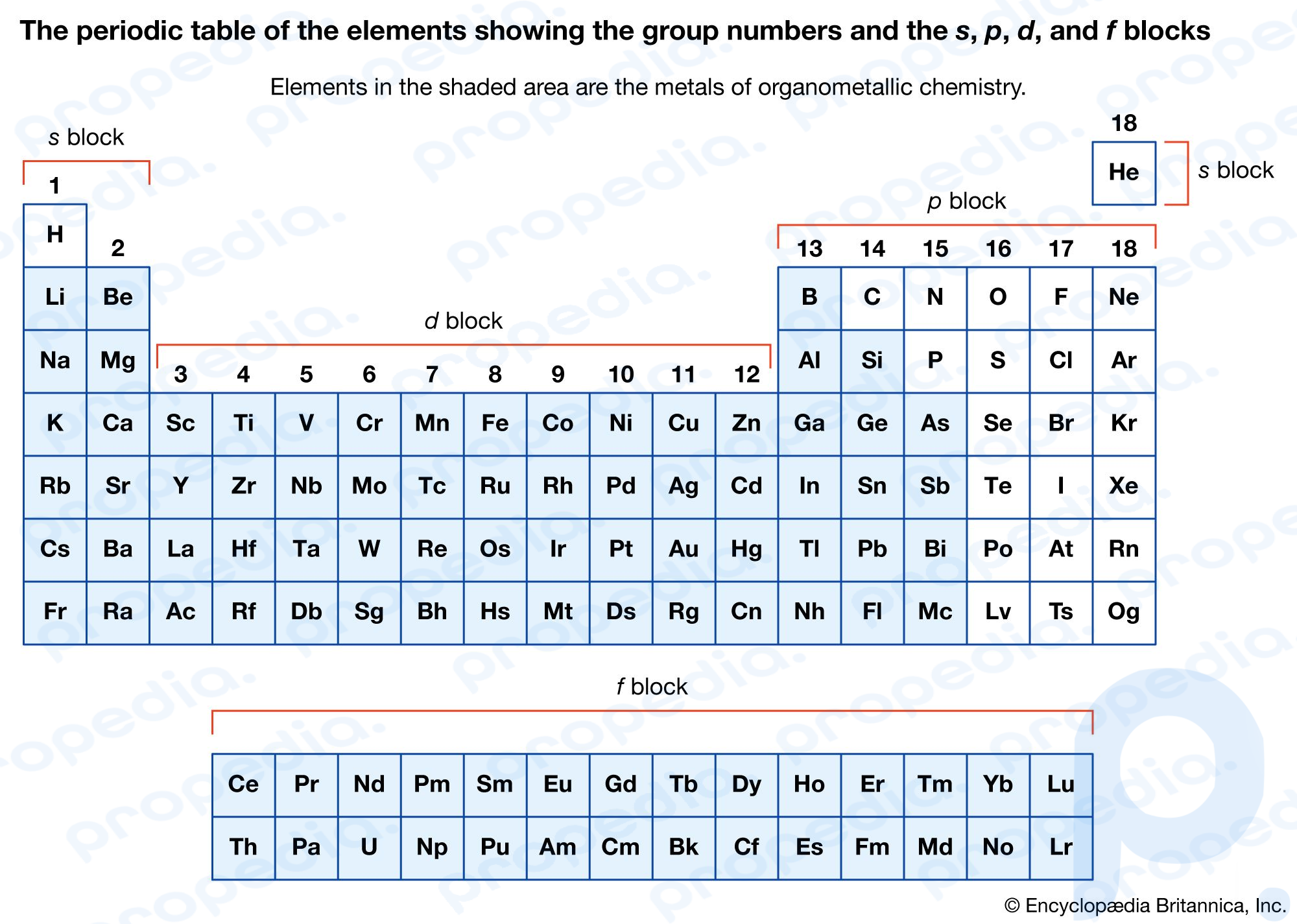
Una aplicación importante de los compuestos de coordinación es su uso como catalizadores, que sirven para alterar la velocidad de las reacciones químicas. Ciertos catalizadores metálicos complejos, por ejemplo, desempeñan un papel clave en la producción de polietileno y polipropileno. Además, una clase muy estable de compuestos de coordinación organometálicos ha impulsado el desarrollo de la química organometálica. Los compuestos de coordinación organometálicos a veces se caracterizan por estructuras "sándwich", en las que dos moléculas de un hidrocarburo cíclico insaturado, que carece de uno o más átomos de hidrógeno, se unen a cada lado de un átomo de metal. Esto da como resultado un sistema aromático altamente estable.
El siguiente artículo cubre la historia, las aplicaciones y las características (incluidas la estructura y los enlaces, los principales tipos de complejos y las reacciones y síntesis) de los compuestos de coordinación. Para obtener más información sobre propiedades específicas o tipos de compuestos de coordinación, consulte los artículos isomería; número de coordinación; reacción química; y compuesto organometálico.
Compuestos de coordinación en la naturaleza.
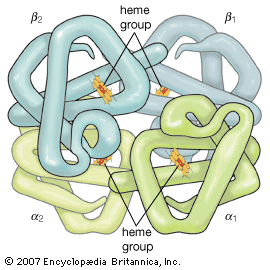
Los compuestos de coordinación naturales son vitales para los organismos vivos. Los complejos metálicos desempeñan una variedad de funciones importantes en los sistemas biológicos. Muchas enzimas, los catalizadores naturales que regulan los procesos biológicos, son complejos metálicos (metaloenzimas); por ejemplo, la carboxipeptidasa, una enzima hidrolítica importante en la digestión, contiene un ion zinc coordinado con varios residuos de aminoácidos de la proteína. Otra enzima, la catalasa, que es un catalizador eficaz para la descomposición del peróxido de hidrógeno, contiene complejos de hierro y porfirina. En ambos casos, los iones metálicos coordinados son probablemente los sitios de actividad catalítica. La hemoglobina también contiene complejos de hierro y porfirina; su papel como transportador de oxígeno está relacionado con la capacidad de los átomos de hierro para coordinar las moléculas de oxígeno de forma reversible. Otros compuestos de coordinación biológicamente importantes incluyen la clorofila (un complejo de magnesio-porfirina) y la vitamina B12, un complejo de cobalto con un ligando macrocíclico conocido como corrina.
Compuestos de coordinación en la industria.
Las aplicaciones de los compuestos de coordinación en química y tecnología son muchas y variadas. Los colores brillantes e intensos de muchos compuestos de coordinación, como el azul de Prusia, los hacen de gran valor como tintes y pigmentos. Los complejos de ftalocianina (p. ej., ftalocianina de cobre), que contienen ligandos de anillos grandes estrechamente relacionados con las porfirinas, constituyen una clase importante de tintes para tejidos.
Varios procesos hidrometalúrgicos importantes utilizan complejos metálicos. El níquel, el cobalto y el cobre se pueden extraer de sus minerales como complejos de amina utilizando amoníaco acuoso. Las diferencias en las estabilidades y solubilidades de los complejos de amina se pueden utilizar en procedimientos de precipitación selectiva que provocan la separación de los metales. La purificación del níquel se puede efectuar mediante reacción con monóxido de carbono para formar el complejo volátil de tetracarbonilníquel, que se puede destilar y descomponer térmicamente para depositar el metal puro. Generalmente se emplean soluciones acuosas de cianuro para separar el oro de sus minerales en forma de un complejo extremadamente estable de dicianoaurato(-1). Los complejos de cianuro también encuentran aplicación en la galvanoplastia.
Hay varias formas en que se utilizan los compuestos de coordinación en el análisis de diversas sustancias. Estos incluyen (1) la precipitación selectiva de iones metálicos como complejos, por ejemplo, el ion níquel(2+) como el complejo de dimetilglioxima (que se muestra a continuación), 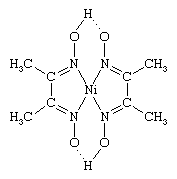 (2) la formación de complejos coloreados, como el ion tetraclorocobaltato(2-). , que se pueden determinar espectrofotométricamente, es decir, mediante sus propiedades de absorción de luz, y (3) la preparación de complejos, como los acetilacetonatos metálicos, que se pueden separar de la solución acuosa mediante extracción con disolventes orgánicos.
(2) la formación de complejos coloreados, como el ion tetraclorocobaltato(2-). , que se pueden determinar espectrofotométricamente, es decir, mediante sus propiedades de absorción de luz, y (3) la preparación de complejos, como los acetilacetonatos metálicos, que se pueden separar de la solución acuosa mediante extracción con disolventes orgánicos.
En determinadas circunstancias, la presencia de iones metálicos no es deseable, como por ejemplo en el agua, en la que los iones de calcio (Ca2+) y magnesio (Mg2+) provocan dureza. En tales casos, los efectos indeseables de los iones metálicos frecuentemente pueden eliminarse "secuestrando" los iones como complejos inofensivos mediante la adición de un reactivo complejante apropiado. El ácido etilendiaminotetraacético (EDTA) forma complejos muy estables y se utiliza ampliamente para este fin. Sus aplicaciones incluyen el ablandamiento del agua (mediante la unión de Ca2+ y Mg2+) y la conservación de sustancias orgánicas, como aceites vegetales y caucho, en cuyo caso se combina con trazas de iones de metales de transición que catalizarían la oxidación de las sustancias orgánicas.
Un avance tecnológico y científico de gran importancia fue el descubrimiento en 1954 de que ciertos catalizadores metálicos complejos, a saber, una combinación de tricloruro de titanio, o TiCl3, y trietilaluminio, o Al(C2H5)3, provocan la polimerización de compuestos orgánicos con compuestos de carbono. dobles enlaces de carbono en condiciones suaves para formar polímeros de alto peso molecular y estructuras altamente ordenadas (estereoregulares). Algunos de estos polímeros son de gran importancia comercial porque se utilizan para fabricar muchos tipos de fibras, películas y plásticos. Otros procesos tecnológicamente importantes basados en catalizadores complejos metálicos incluyen la catálisis mediante carbonilos metálicos, como el hidradotetracarbonilcobalto, de la llamada hidroformilación de olefinas (es decir, de sus reacciones con hidrógeno y monóxido de carbono para formar aldehídos) y la catálisis mediante tetracloropaladato(2). −) iones de oxidación de etileno en solución acuosa a acetaldehído ( ver reacción química y catálisis).
